Radiant™ Aura erhält die 510(k)-Zulassung der US-amerikanischen Food and Drug Administration (FDA).
Erweitert die praxisnahen Behandlungsmöglichkeiten für Millionen von Patienten mit nicht-melanozytärem Hautkrebs (NMSC).
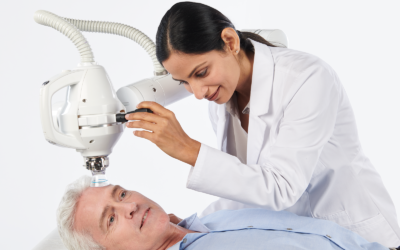
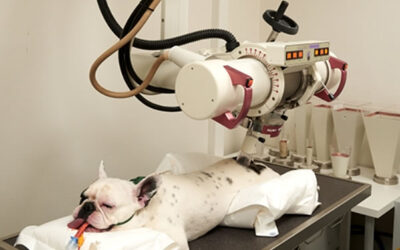
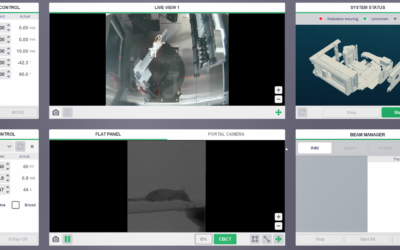
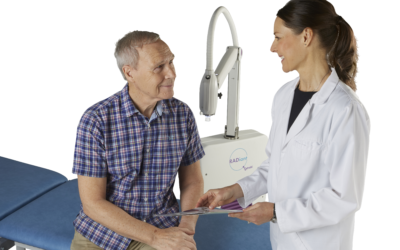
Xstrahl, ein weltweit führender Anbieter von oberflächlichen Strahlentherapiegeräten und präklinischen Strahlenforschungssystemen, gab seine bekannt Radiant™ Aura-Behandlungslösung hat die 510(k)-Zulassung der US-amerikanischen Food and Drug Administration (FDA) erhalten. Mit erweiterten Funktionen für erweiterten klinischen Einsatz, vereinfachter Patientenpositionierung und zusätzlichem Patientenkomfort. Radiant Aura bietet NMSC-Patienten Strahlentherapie in jeder Hautarztpraxis.
Downloads
Ressourcentyp: Produktinformationen
Kontakt