Radiant™ Aura reçoit l'autorisation 510(k) de la Food and Drug Administration (FDA) des États-Unis
Élargit les options de traitement en cabinet pour des millions de patients atteints d'un cancer de la peau autre que le mélanome (NMSC)
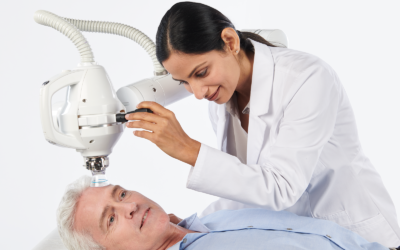
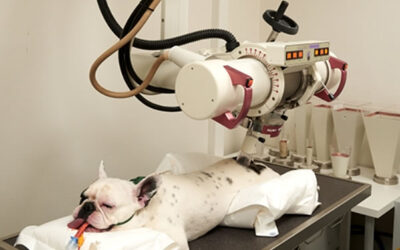
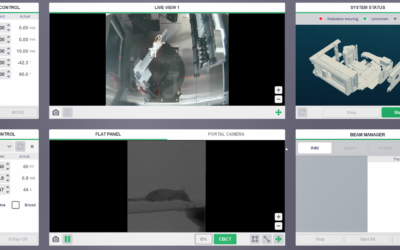
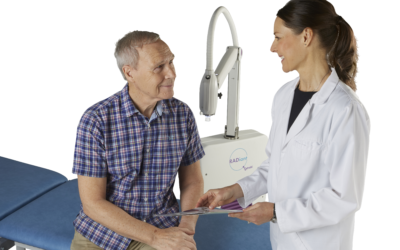
Xstrahl, un leader mondial dans la fourniture d'appareils de radiothérapie superficielle et de systèmes de recherche préclinique sur les rayonnements, a annoncé son Radiant™ La solution de traitement Aura a reçu l'autorisation 510(k) de la Food and Drug Administration (FDA) des États-Unis. Avec des fonctionnalités avancées pour une utilisation clinique étendue, un positionnement simplifié du patient et un confort accru pour le patient, Radiant Aura apporte la radiothérapie aux patients NMSC dans n'importe quel bureau de dermatologie.
Resources
Type de ressource : Informations sur le produit
Contactez-Nous